Pembentukan Ikatan Ion
Bila atom yang mempunyai energi ionisasi rendah berdekatan dengan atom yang mempunyai affinitas elektron besar maka akan terjadi perpindahan elektron dari atom yang berenergi ionisasi rendah ke atom yang mempunyai affinitas elektron besar.
Contoh:
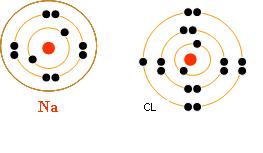
1. ikatan yang terjadi antara 11Na dengan 17Cl .
Konfigurasi elektron masing-masing atom:
11Na : 2 8 1
17Cl : 2 8 7
1. ikatan yang terjadi antara 11Na dengan 17Cl .
Konfigurasi elektron masing-masing atom:
11Na : 2 8 1
17Cl : 2 8 7
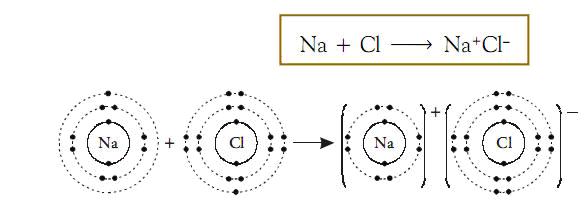
Atom natrium melepas 1 elektron kulit terluarnya, sehingga konfigurasi elektronnya sama dengan gas mulia. Atom klorin menerima satu elektron pada kulit terluarnya sehingga konfigurasi elektronnya sama dengan gas mulia .
Akibatnya atom Na akan berubah menjadi ion positif dan atom Cl berubah menjadi ion negatif. Dan kedua ion ini saling berinteraksi dengan gaya elektrostatika sebagai berikut:
Akibatnya atom Na akan berubah menjadi ion positif dan atom Cl berubah menjadi ion negatif. Dan kedua ion ini saling berinteraksi dengan gaya elektrostatika sebagai berikut:

Ikatan yang terjadi antara Ion positip Na dan Ion negatif Cl disebut ikatan ion.
Sifat umum senyawa ionik:
1. Berbentuk Kristal
Sifat umum senyawa ionik:
1. Berbentuk Kristal
Kristal inilah yang menyebabkan senyawa yang berikatan ion memiliki titik leber tinggi.
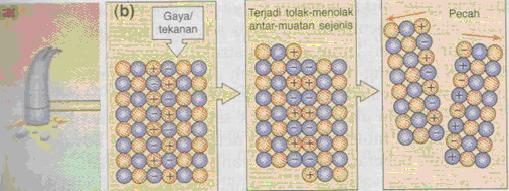
1. Keras tapi rapuh
1. Keras tapi rapuh
1. Lelehannya dapat menghantarkan listrik
Karena ion – ion dapat bergerak bebas apabila dalam bentuk lelehan.
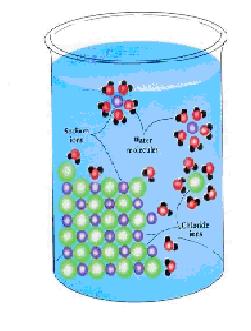
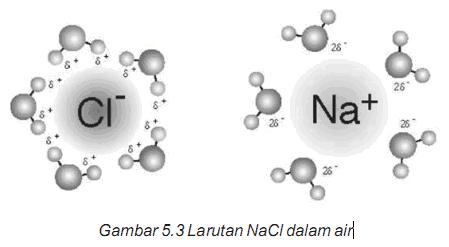
2. Larut dalam air dan bersifat elektrolit.
Karena ion – ion dapat bergerak bebas apabila dalam bentuk lelehan.
2. Larut dalam air dan bersifat elektrolit.